Vanaf 1 december 2020 verandert de procedure voor het indienen van een lokale uitvoerbaarheidsverklaring voor medisch-wetenschappelijk onderzoek, de zogenaamde procedure Lokale haalbaarheid. De nu geldende Onderzoeksverklaring is in de nieuwe werkwijze vervangen door de Verklaring Geschiktheid Onderzoeksinstelling (VGO). De aangepaste procedure gaat gelden voor al het WMO-plichtige onderzoek in Nederland en is van toepassing op zowel multicenter- als monocenteronderzoek. De CCMO past op dit moment de Richtlijn Externe Toetsing aan op deze wijziging. Het gebruik van de VGO wordt verplicht vanaf 1 juni 2021. De periode 1 december 2020 – 1 juni 2021 geldt als overgangsperiode waarin opdrachtgevers kunnen kiezen of ze voor de toetsing van de geschiktheid van de deelnemende centra gebruik maken van de Onderzoeksverklaring of de VGO.
Lokale haalbaarheid
Kort samengevat zorgt de nieuwe werkwijze ervoor dat het nagaan van de haalbaarheid in de deelnemende instellingen al geregeld is vóórdat de toetsingscommissie het onderzoeksdossier beoordeelt, in plaats van – zoals nu –daarna. Op die manier kan de inclusie van proefpersonen meteen beginnen zodra de toetsingscommissie een positief oordeel over een onderzoek heeft gegeven. Daardoor wordt de opstarttijd van onderzoek aanzienlijk korter en de inclusieperiode optimaal benut.
Om de nieuwe procedure te kunnen volgen zijn de volgende documenten beschikbaar:
- Formulier Verklaring Geschiktheid Onderzoeksinstelling (VGO) (Word-versie),
- Formulier Verklaring Geschiktheid Onderzoeksinstelling (VGO) (PDF-versie),
- Model Onderzoekscontract (CTA), behorend bij nieuwe procedure lokale haalbaarheid.
Schematische weergave van de stappen in de Procedure Lokale haalbaarheid
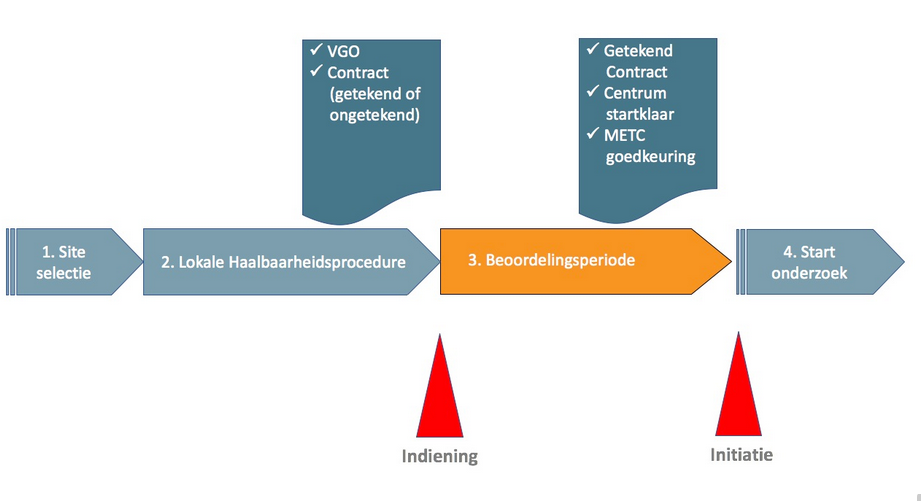
Verklaring geschiktheid Onderzoeksinstelling (VGO)
Met de nieuwe werkwijze hebben opdrachtgevers van zowel bedrijfsgeïnitieerd als onderzoeker geïnitieerd onderzoek de taak om de details van het onderzoek weer te geven in een onderzoek specifieke VGO en deze aan te leveren bij de deelnemende onderzoeksinstellingen. De VGO bestaat uit een Deel A en Deel B. In de bijlagen van Deel B geeft de opdrachtgever de informatie over de benodigde onderzoeksverrichtingen per ondersteunende afdeling.
De lokale hoofdonderzoeker gaat aan de hand van de informatie in de VGO en de finale versie van het onderzoeksprotocol, in het eigen centrum de lokale haalbaarheid na, en legt dit vast in Deel B van de VGO. Dit dient als informatiebron voor de Raad van Bestuur, die vervolgens Deel A ondertekent. Met de ondertekening van Deel A verklaart de Raad van Bestuur dat de instelling geschikt is het onderzoek uit te voeren.
Het lokale haalbaarheidsoverleg dient plaats te vinden vóór indiening van het onderzoek bij de toetsingscommissie (zie plaatje), omdat het ondertekende Deel A van de VGO onderdeel is van het toetsingsproces.
Opdrachtgevers die vanaf 1 december 2020 gebruik willen maken van de nieuwe procedure dienen voor ieder deelnemend centrum een getekend deel A van de VGO én een onderzoekscontract overeenkomstig de nieuwe procedure in te dienen.
Standaard onderzoekscontract (CTA)
Bij het volgen van de nieuwe procedure is het noodzakelijk het standaard onderzoekscontract (CTA) te gebruiken, waarin ‘opschortende voorwaarden’ zijn beschreven. Met ondertekening van dit contract geeft de Raad van Bestuur van de onderzoeksinstelling voorwaardelijk toestemming voor uitvoering van het onderzoek. Dit betekent dat het onderzoek pas kan worden uitgevoerd als aan deze voorwaarden is voldaan. De standaard voorwaarde is goedkeuring van het onderzoek door een toetsingscommissie. De herziene template van het CTA, met deze ‘opschortende voorwaarden’, is vanaf 1 december beschikbaar via de website van de CCMO, net als het huidige CTA.
Met deze werkwijze komt de brief met de toestemming van de Raad van Bestuur te vervallen. De praktijk heeft geleerd dat deze brief veel vertraging oplevert bij het opstarten van het onderzoek in onderzoeksinstellingen.
Aanpassing nodig vanwege ECTR
De aanleiding voor het aanpassen van de procedure voor het indienen een lokale uitvoerbaarheidsverklaring, is de EU-verordening voor geneesmiddelenonderzoek, ook wel bekend als de European Clinical Trial Regulation (ECTR), die naar verwachting in december 2021 van toepassing wordt.
De Procedure Lokale haalbaarheid is ontworpen door de DCRF-werkgroep Lokale uitvoerbaarheid, in samenwerking met vertegenwoordigers van de betrokken veldpartijen, de CCMO en wetenschappelijke verenigingen. De procedure bestaat uit vier stappen met verantwoordelijkheden en activiteiten voor de opdrachtgever, de lokale hoofdonderzoeker, de Raad van Bestuur van de onderzoeksinstelling, en de toetsingscommissie. Deze stappen staan in meer detail uitgewerkt op de pagina Lokale haalbaarheid van de DCRF-website.
Hieronder staan de documenten die opdrachtgevers, onderzoekers en andere klinisch onderzoek professionals ondersteuning bieden:
Evaluatie nieuwe procedure
De DCRF en de CCMO zullen de nieuwe lokale haalbaarheidsprocedure en het gebruik van de VGO samen evalueren. De resultaten hiervan bepalen of de procedure nog aanpassingen behoeft. Deze evaluatie zal uiterlijk 1 december 2021 afgerond zijn. Om die reden willen de leden van de DCRF-werkgroep Lokale uitvoerbaarheid graag ervaringen horen over het werken volgens de procedure en het gebruik van de VGO.
Alle vragen en reacties zijn welkom. Alleen met inbreng van de gebruikers kunnen we de procedure optimaliseren. Stuur je reacties daarom naar secretariaat@dcrfonline.



